用紫外分光光度法测定饮料中的总 D-异柠檬酸的含量
发布时间:2019-02-26 点击次数:0
1 范围 侵删,请告知
本方法采用紫外分光光度法测定橙、柑桔汁饮料中总 D-异柠檬酸的含量。
本方法适用于橙、柑桔汁饮料中总 D-异柠檬酸的测定,以 mg/kg报告其结果,测定值保
留一位小数。
2 原理
在异柠檬酸脱氢酶(ICDH)催化下,样品中的D-异柠檬酸盐与烟酰胺-腺嘌呤-双核苷酸
磷酸(NADP)作用,生成NADPH的含量,相当于D-异柠檬酸盐的量。在波长340 nm处测定
吸光度,确定样品中总D-异柠檬酸的含量。
3 试剂
3.1 组合试剂盒(Cat No.414433)
1 号瓶:内含咪唑缓冲液(稳定剂)30 mL,pH=7.1;
2 号瓶:内含β-烟酰胺-腺嘌呤-双核苷酸-磷酸二钠45 mg、硫酸锰10 mg;
3 号瓶:内含异柠檬酸脱氢酶2 mg,5(U)个活力单位。
3.2 NADP溶液:
将1号瓶内的溶液升温至20~25℃,倒入2号瓶中,使2号瓶的物质全部溶解,
混合均匀。
3.3 异柠檬酸脱氢酶溶液
用1.8 mL水溶解3号瓶的物质,混合均匀。
3.4 氢氧化钠溶液,4 mol/L
称取16 g氢氧化钠,加水溶解,定容至100 mL。
3.5 盐酸溶液,4 mol/L
量取33.4 mL盐酸,用水定容至100 mL。
3.6 氯化钡溶液,300 g/L
称取30 g氯化钡,溶解于热水中,冷却后定容至100 mL。
3.7 硫酸钠溶液,71 g/L
称取71 g无水硫酸钠,溶解于水中,定容至1000 mL。
3.8 缓冲溶液
称取2.4 g三羟甲基氨甲烷和0.035 g乙二胺四乙酸二钠,用80 mL水溶解。先用4 mol/L的
盐酸调整pH=7.2左右,再用1 mol/L盐酸溶液调整pH=7.0(用酸度计测定),用水定容至100 mL。
3.9 氨水
3.10 丙酮
3.11 洗涤溶液
量取150 mL水,加入10 mL氨水(3.9)、100 mL丙酮(3.10),混匀。
4 仪器与设备
4.1 紫外分光光度计
带石英比色皿,光程1 cm。
4.2 酸度计,精度0.1 pH单位
4.3 离心机
转速不低于4000 r/min,离心管容积大于80 mL。
4.4 微量可调移液管
10~50μL,允许误差(%):±4.8;
2
0~1000μL,允许误差(%):100μL,±2.0;500μL,±1.0;1000μL,±1.0。
4.5 玻璃棒或塑料棒
自制,直径约3 mm,一端带钩。
5 操作步骤
5.1 试液的制备
5.1.1 果汁型碳酸饮料:称取500 g样品于1000 mL烧杯中,加热煮沸,在微沸状态下保持5
min,并不断搅拌。待二氧化碳基本除净后冷却至室温,称量。用水补足至加热前的质量,备
用。
5.1.2 浓缩果汁、果汁、果汁饮料、水果饮料:混匀后备用。
5.2 水解
按表1规定的取样量称取试液
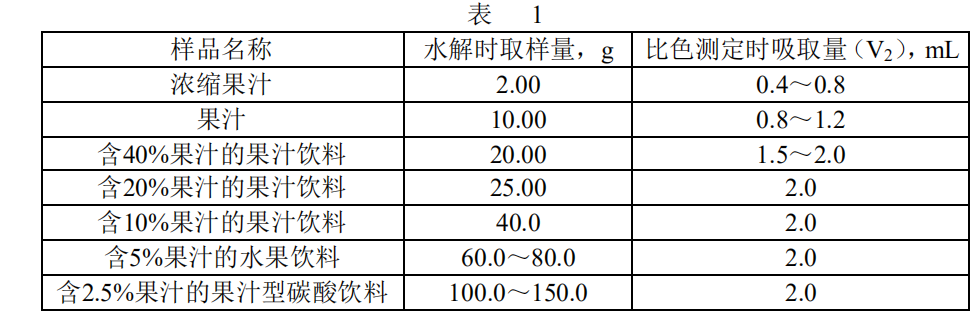
浓缩汁、果汁:将试样称取在50 mL烧杯中,加5 mL氢氧化钠溶液(4 mol/L)。用玻璃棒
搅拌均匀,在室温放置10 min,使之水解。将溶液移入离心管中,用5 mL盐酸酸溶液(4 mol/L)
和10~20 mL水,分数次洗涤烧杯,并入离心管中,使总体积约为30 mL,搅拌均匀。
果汁饮料、水果饮料、果汁型碳酸饮料:将试液称取在离心管中,加5 mL氢氧化钠溶液
(4mol/L),用玻璃棒搅拌均匀,在室温放置10 min,使之水解。加5 mL盐酸溶液(4 mol/L),
搅拌均匀。
5.3 沉淀
5.3.1 称样量小于或等于25 g的试液
在盛有水解物的离心管中依次加入2 mL氨水、3 mL氯化钡溶液(300 g/L)、20 mL丙酮,
用玻璃棒搅拌均匀。取出玻璃棒,按顺序摆放在棒架上。将离心管在室温(约20℃)放置10 min,
以3000 r/min转速,离心5~10 min,小心倾去上层溶液,保留离心管底部沉淀物。
5.3.2 称样量大于25 g的试液
按5.2和5.3.1的步骤分别制备2~6份沉淀物,然后用约50 mL洗涤溶液将2只(或3只、4只、
6只,视称样量而定)离心管中的沉淀物合并到1只离心管中,在室温(约20℃)放置10 min。
以下步骤按5.3.1操作。
5.4 溶解
将5.3中取出的玻璃棒按顺序放回原离心管中,向离心管中加入20 mL硫酸钠溶液(71
g/L)。将离心管置于微沸水浴中加热10 min,同时用玻璃棒不断搅拌。趁热用缓冲溶液将离
心管中的内容物转移至50 mL容量瓶中。冷却至室温(约20℃)后用缓冲溶液定容至刻度,摇
匀。
5.5 将上述溶液用滤纸过滤,弃去最初滤液,保留滤液备用。
5.6 测定
5.6.1 测定条件
波长:340 nm;温度:20~25℃;比色浓度:在0.1~2.0 mL试液中,含D-异柠檬酸3~
100μg。
5.6.2 测定步骤
3
按表2规定的程序和溶液的加入量,用微量可调移液管依次将各种溶液加入比色皿中(微
量可调移液管须用吸入溶液至少冲洗一次,再正式吸取溶液),立即用玻璃棒上下搅拌,使比
色皿中的溶液充分混匀。
加异柠檬酸脱氢酶溶液后的最终体积为3.05 mL。
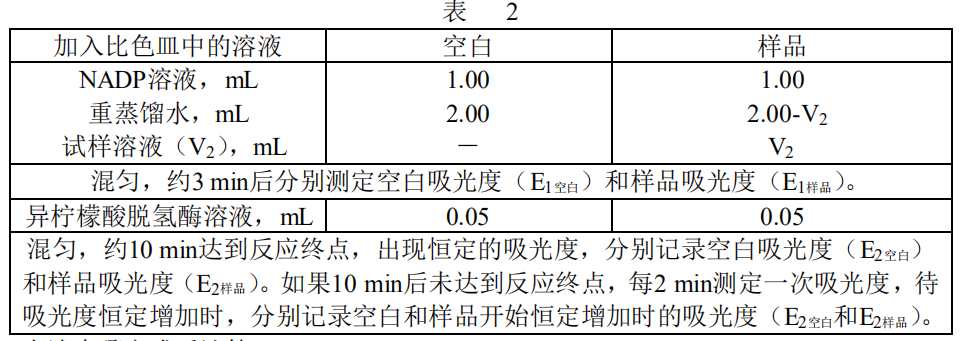
上述步骤完成后计算ΔE:
E ( E ) ( E ) DE = DE样品 - D 空白 = E2样品 - 1样品 - E2空白 - 1空白
为得到精确的测定结果,ΔE必须大于0.100。如ΔE小于0.100,应增加水解时的取样量或
增加比色时的吸取量。
5.6.3 异柠檬酸脱氢酶活力的判定方法
5.6.3.1 D-异柠檬酸标准溶液
称取
P
0.0153
g、含有2个结晶水的D-异柠檬酸三钠盐(C6H5Na3·2H2O)基准试剂,精确
至0.0001 g。置于50 mL烧杯中。加水溶解,转移到100 mL容量瓶中,用水定容至刻度,摇匀,
贮存于冰箱中。此溶液含D-异柠檬酸为100 mg/L。
P为D-异柠檬酸基准试剂的纯度(百分含量)。0.0153为系数,按下式计算得出
0.0153
192.1( ) 1000
294.1( 2 ) 100( ) 0.1( )
6 5 7 3 2
=
- ´
· ´ ´ -
异柠檬酸的分子量
的分子量 稀释体积 异柠檬酸的浓度
D
C H O Na H O D
5.6.3.2 酶活力与标样吸潮的判定
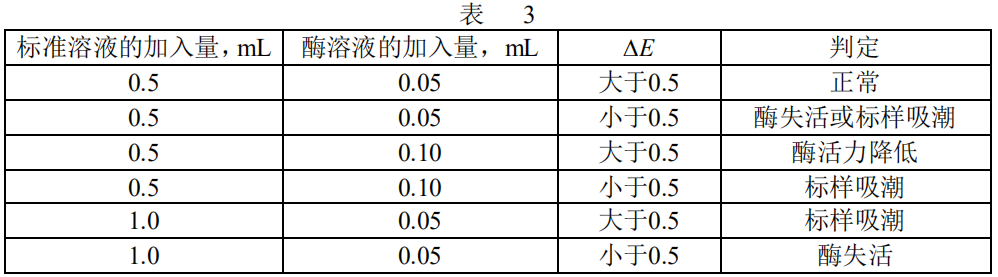
若酶活力降低,应控制测定样品的ΔE,使之小于标样的ΔE,以保证测定样品中总D-异
柠檬酸反应完全。
6 结果计算
样品总D-异柠檬酸的含量按下式计算:
E
m V
V
x ´ D
´ ´ ´
´ ´
=
6.3 1 '
3.05 192.1
式中:x— — 样品中总D-异柠檬酸的含量,mg/kg;
4
3.05— — 比色皿中溶液的最终体积,mL;
192.1— — D-异柠檬酸的分子质量,g/mol;
V— — 试液的定容体积,mL;
V’— — 比色测定时吸取滤液的体积,mL;
m— — 样品的质量,g;
1— — 比色皿光程,cm;
6.3— — 反应产物NADPH在340 nm的吸光系数,1×mmol-1
cm-1。
7 允许差
同一样品的两次测定结果之差,果汁含量等于或大于10%的样品,不得超过平均值的
5.0%;果汁含量2.5%~10.0%的样品,不得超过平均值的10.0%。
8 参考文献
GB/T 16771-1997“橙、柑、桔汁及其饮料中果汁含量的测定”附录 D“总 D-异柠檬酸的
测定
上一条:柠檬酸钠的技术要求与试验标准
下一条:用滴定法_比色法测验柠檬酸